
6 protoner (røde) og 6 nøytroner (blå)
Karbon er et grunnstoff i naturen med forkortelsen (kjemisk tegn) C. Vi finner det både i diamanter, i spissen på blyanten, i kull og i alle levende organismer. Det vanligste karbon-atomet har 6 protoner og 6 nøytroner i kjernen, tilsammen 12 - derfor kalles det C12. Av alt karbon i verden er omtrent 98,9% C12.
Isotoper
Men det finnes 2 varianter til av karbon. De kalles isotoper. Den ene isotopen er et atom som har 6 protoner, men 7 nøytroner i kjernen, til sammen 13. Derfor kalles isotopen C13. Det utgjør omlag 1,1% av alt karbon.
Nitrogen har 7 protoner (røde) og 7 nøytroner (blå)
Så er det den siste isotopen. Og fordi den heter C14, har du sikkert skjønt at den har 14 kjerne-elementer til sammen - 6 protoner og 8 nøytroner. Denne isotopen lages i atmosfæren ved hjelp av stråling fra verdensrommet. Det er en veldig liten del av alt karbonet som er C14, bare 0,0000000001%! Tenk deg at du la milliarder av kronestykker ut over hele jordens overflate, slik at den ble helt dekket. Hvis du tenker deg at alle kronestykkene er karbon-atomer, så ville bare ETT av dem være en C14-isotop!
Et N-atom som har lyst å være C
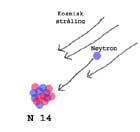
Nitrogenatomet blir truffet av et nøytron
C14-isotopen er opprinnelig et nitrogen-atom (N14) som normalt har 7 protoner og 7 nøytroner i kjernen. Det er fordi det har 7 protoner i kjernen at det er et nitrogen-atom. Hadde det hatt 6 protoner, hadde det vært et karbon-atom. Men det er akkurat det som hender når kjernen i nitrogen-atomet blir truffet av frie nøytroner som kommer mot jorda i den kosmiske strålingen fra verdensrommet.
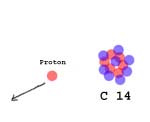
Protonet er sparket ut, og nitrogen er blitt karbon.
Disse nøytronene treffer nitrogenkjernen og "sparker" ut ett av protonene! Da blir det bare 6 protoner igjen i kjernen, men til gjengjeld er det nå 8 nøytroner! Da er atomet plutselig blitt et karbon-atom (6 protoner=karbon) med 14 kjerne-elementer - det er blitt en C14-isotop.
C14-isotopene går inn i kroppene
I atmosfæren vil C14-isotopene straks søke sammen med oksygen (O) og danne CO2-gass. Plantene bruker den til å lage oksygen, og når dyr og mennesker spiser planter og dyr som mat, vil etter hvert alle levende vesener få en stabil konsentrasjon av C14. Når noe av C14-atomene forsvinner, kommer nye isotoper til, slik at forholdet alltid er det samme så lenge vi lever. Men når vi dør, slutter vi å ta opp C14 gjennom maten og luften.
Har lyst å bli N-atom igjen
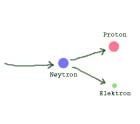
Nøytronet splittes i et proton og et elektron
I naturen søker alt tilbake til likevekt, og C14-isotopen er veldig ustabil. Den vil gjerne bli et stabilt nitrogenatom igjen. Og det blir den! Det skjer ved at et av nøytronene plutselig forandrer seg til to nye elementer - et proton og et elektron. Protonet blir igjen i kjernen, så nå er det på nytt blitt 7 protoner og 7 nøytroner der - altså et stabilt nitrogenatom (N14).
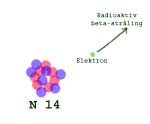
Elektronet fyker ut som beta-stråling, og atomet er blitt nitrogen igjen.
Elektronet sendes ut fra atomkjernen med voldsom kraft - det kaller vi beta-stråling. "Stråle" heter "radio" på latin, og derfor sier vi at C14-isotopen er radioaktiv og at den sender ut radioaktiv stråling.
Halveringstid
Når vi har et stort antall C14-atomer, er tiden det tar før halvparten av alle disse C14-isotopene er omdannet til nitrogen-atomer igjen, alltid den samme: 5.570 år. Det vil si at på 5.570 år er mengden C14 redusert til halvparten, etter 11.140 år er den en firedel, etter 16.710 år en åttedel og så videre. Vi kaller denne måle-enheten halveringstid. Alle radioaktive isotoper har en målbar halveringstid. Den kan variere fra bare noen brøkdeler av et sekund opp til millioner av år, avhengig av typen isotop.
Vi teller C14-isotoper
Siden levende organismer slutter å ta opp C14 når de dør, kan vi finne ut hvor gamle de er ved å måle konsentrasjonen av C14 i dem. Så kan vi sammenligne den med den normale konsentrasjonen av C14 i et levende individ. Og når vi har forskjellen mellom de to mengdene, kan vi finne ut hvor gammelt f.eks. treet eller menneskebeinet er. For vi vet jo hvor lang tid det tar før mengden av C14 er halvert - 5.570 år. Resten kan vi regne ut med enkel matematikk eller bruke tabeller som andre har laget for oss.
Hvordan måler vi?
Hvordan måler vi konsentrasjonen av C14 i for eksempel et menneskebein? Det er to måter å gjøre det på, men her skal vi forklare den måten NTNU i Trondheim gjør det på. Vi bruker et telleapparat som huker tak i elektronene som stråles ut fra C14-isotopen - beta-partiklene - og teller dem. Antallet elektroner forteller oss hvor mange C14-isotoper som er til stede.
Referansen vår
Hvordan vet vi hvor mange C14-isotoper som dannes til en hver tid i atmosfæren - det som er 100%-nivået? Jo, det er den kosmiske strålingen som forårsaker dannelsen av isotopene. Hvis den kosmiske strålingen hadde vært den samme år etter år, hadde det vært enkelt å finne ut "normaltallet" for C14-isotopene i atmosfæren. Men dessverre for oss varierer strålingen hele tiden.
Gamle trær hjelper oss
Hva gjør vi da? Jo, vi finner oss et veldig gammelt tre - 11.000 år gamle trær kan vi faktisk finne. Så måler vi mengden C14 i hver av årringene i treet, og kan på den måten finne ut hvordan den kosmiske strålingen har variert 11.000 år tilbake i tiden. Så "retter" vi måleresultatene etter dette, slik at vi har et "normaltall" å gå etter.
Nye problemer
Men problemene er ikke over for det. For måleapparatet vårt er jo utsatt for kosmisk stråling mens det måler! Og i den kosmiske strålingen er det også beta-partikler. Da blir det jo feil i målingene! Først må vi beskytte måleapparatet mot strålingen så godt vi kan (vi setter det i et tilfluktsrom og pakker det inn i jernplater), så måler vi med et annet apparat hvor mange kosmiske beta-partikler som trenger inn - og trekker det fra målingene våre.
Å kalibrere
Til slutt må vi sammenligne våre målinger med målinger fra noe vi kjenner alderen på. Alt dette kalles å kalibrere målingene. Tiden målingene (eller tellingene) tar, varierer etter størrelsen og alderen på prøvene. Store prøver (på for eksempel 5 liter gass) tar 16-17 timer å telle, gamle og små prøver kan ta opp til en uke å telle.
Slik måler vi bein
Når vi teller C14-isopenes utstrålte beta-partikler i menneske-bein, er det det organiske bindevevet i beinet vi tar ut fordi det ikke blir forurenset av andre ting. Det blir nemlig resten av beinet! For å få det til, må vi behandle beinet med mange forskjellige kjemikalier og prosesser. Til slutt blir beinet brent, og vi tar vare på gassen som oppstår. Da først kan C14-tellingen starte.
Til tross for alle kalibreringene og korreksjonene, er ikke den alderen vi kommer fram til sikrere enn cirka 68%. Det vil si at det er 68% sannsynlighet for at gjenstanden er så gammel som C14-målingene viser. Det er likevel godt nok for oss og beinet vårt!





