
Rot i systemet
Periodesystemet har holdt orden på grunnstoffene i 150 år, men under den ryddige overflata er det enkelte ting som skurrer.
Noen grunnstoff er kjente – for eksempel jern (Fe) og fluor (F), noen er kjære – gull (Au) og sølv (Ag). Enkelte er forbeholdt de spesielt interesserte, har du hørt om flerovium (Fl) eller praseodym (Pr)? Noen er så å si overalt, Jordas atmosfære består nesten utelukkende av nitrogen (N) og oksygen (O). Andre oppstår kun flyktig under helt spesielle forutsetninger i et laboratorium, for eksempel nihonium (Nh) og oganesson (Og).
Enkelte grunnstoff er nødvendige for alt liv vi kjenner til, uten karbon (C) hadde vi ikke kommet langt. Tenness (Ts) hadde vi nok derimot klart oss helt fint uten.
De 118 grunnstoffene er brikkene som utgjør puslespillet vi kjenner som periodesystemet. Men ikke alle brikkene passer like perfekt.
Mendelejev-myten
Kjemikeren Dmitrij Mendelejev var i 1869 professor i St. Petersburg. Selv hadde han full kontroll på de 63 grunnstoffene man kjente til på den tida, men han mangla oppdaterte lærebøker han kunne bruke i undervisninga. Han jobba med sitt eget lærebokverk – første bind hadde kommet ut året før, men nå sto han fast. Hvordan skulle kapitlene organiseres? Hvilke grunnstoff hørte til i hvilke kapitler?
Myten sier at kabalentusiast Mendelejev en mandagsmorgen for ganske nøyaktig 150 år siden prøvde seg på en ny tilnærming til problemet. Hvert grunnstoff fikk sitt eget kort der han skrev ned stoffets grunnleggende egenskaper. På denne måten kunne han enkelt flytte kortene rundt på bordet og se etter sammenhenger.
Mendelejev skal deretter ha sovna, og sett hvordan grunnstoffene passa sammen i en drøm. Så fort han våkna, skrev han ned et tilnærma ferdig system. En fenomenal vitenskapelig åpenbaring – lett å gjenfortelle, men vanskelig å tro på. Akkurat som da Newton beleilig nok fikk et eple i hodet og plutselig forsto tyngdekraft.
Svært lite tyder på at noe av dette faktisk skjedde. Den mindre kjente, men veldig mye mer sannsynlige forklaringa, er at han gjorde som forskere stort sett gjør – prøvde og feila, over lang tid, til han fikk det til å stemme. Det var nok også tilfellet for Newtons del.

Grunnstoff nummer 101, mendelevium, er oppkalt etter Mendelejev. Det er også krateret Mendeleev, som ligger på Månen.
Det som er sikkert er at Mendelejev sendte artikkelen Et forsøk på et grunnstoffsystem basert på deres atomvekt og kjemiske slektskap til trykking.
Forsøket på å systematisere skulle vise seg å være særdeles solid. Det skapte ikke umiddelbart oppstuss i kjemiverdenen, men la grunnlaget for tabellen som fortsatt henger i klasserom verden over. Men kommer tabellen fortsatt til å se lik ut om 100 år?
Fra hydrogen til oganesson
For å forstå hvorfor periodesystemet ser ut som det gjør, og hvorfor det eventuelt bør forandres, må vi starte med noe av det aller mest grunnleggende vi har: grunnstoffene. Dette er barnelærdom, men sannsynligvis også glemt barnelærdom for mange, så vi koster på oss ei grundig oppfriskning:
Definisjonen på et grunnstoff er et stoff som bare består av én type atomer. Atomene er bygd opp av enda mindre partikler – en kjerne av protoner og nøytroner, med elektroner som surrer rundt i ett eller flere elektronskall.
Hydrogen, som er grunnstoff nummer én, har ett proton i kjernen, og ett elektron som surrer rundt. Helium, grunnstoff nummer to, har to protoner i kjernen, og to elektroner som snurrer rundt. Jern, grunnstoff nummer 26, har 26 protoner i kjernen og 26 elektroner som snurrer rundt. Man trenger ikke være Mendelejev for å ane et mønster her, men han hadde ikke mulighet til å forholde seg til protoner og elektroner, av den enkle grunn at de fortsatt ikke var oppdaga.
Hydrogen
Helium
Jern
Det Mendelejev derimot forholdt seg til var atomvekt. Som hovedregel øker den med antallet protoner i atomkjernen, det ville altså ikke vært noe problem å systematisere grunnstoffene i ei liste, fra lettest til tyngst.
Problemet med ei sånn liste er at den da bare ville sagt noe om grunnstoffenes fysiske egenskaper. Mendelejev ville også inkludere de kjemiske egenskapene – hvordan stoffene reagerer med andre stoffer. Han visste for eksempel at fluor, klor, brom og jod kunne minne om hverandre i måten de oppfører seg på, til tross for at de ikke ligger i nærheten av hverandre vektmessig.
Et alternativ til å pugge periodesystemet er å lære seg en snaut tre minutter lang sang.
Fullt skall, takk
Ved å kombinere kjemi og fysikk kom Mendelejev fram til det systemet vi har bygd videre på i 150 år – et system basert på grupper og perioder.
Når vi nå skal se nærmere på hvordan periodesystemet er oppbygd forlater vi Mendelejevs variant, og tar for oss 2019-varianten. Selv om hovedprinsippet i systemet fra 1869 fortsatt står seg, er begrunnelsene annerledes.
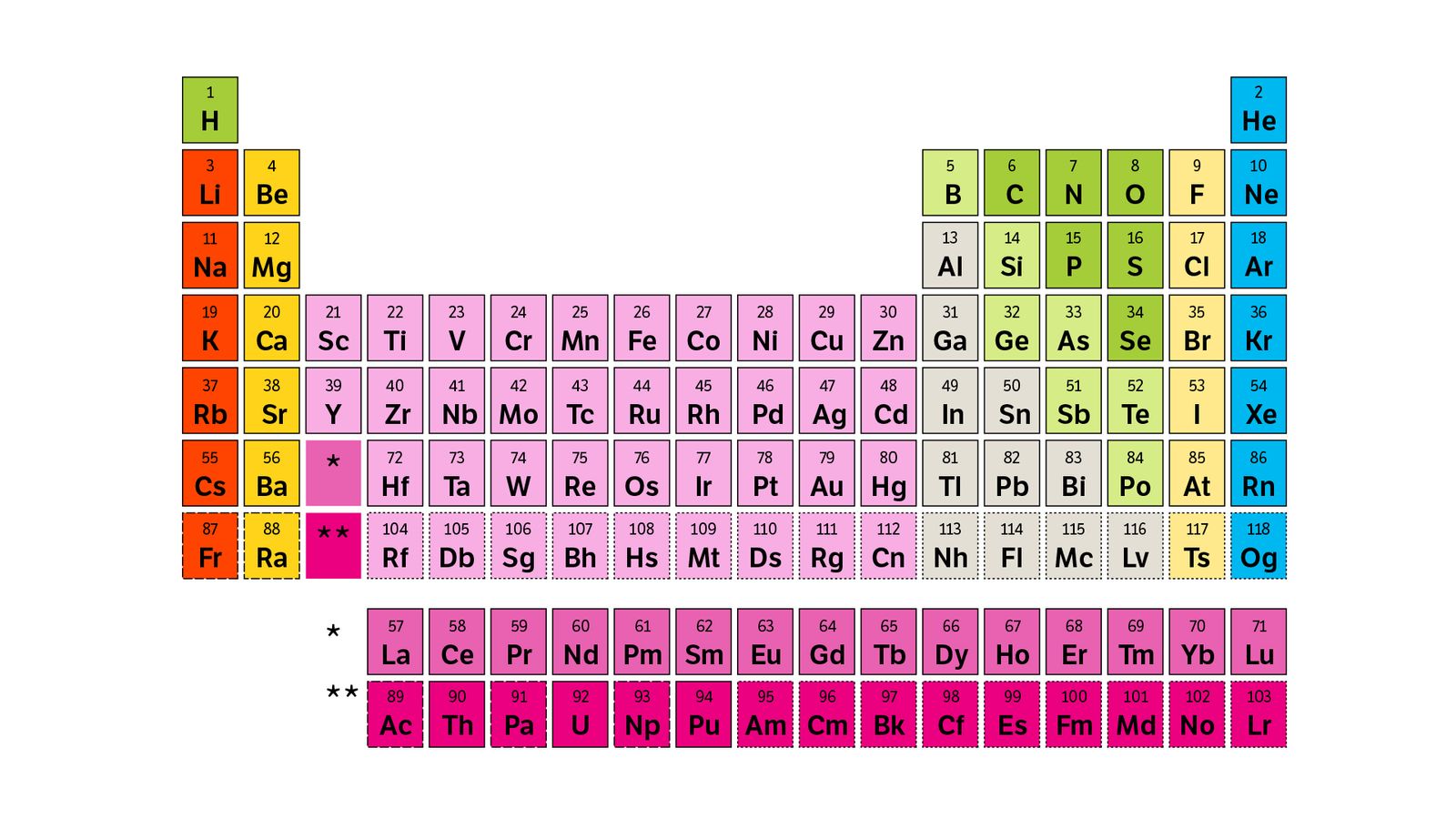
De 18 forskjellige gruppene står i vertikale rader, og litt enkelt sagt har grunnstoff i samme gruppe like mange elektroner i det ytterste elektronskallet.
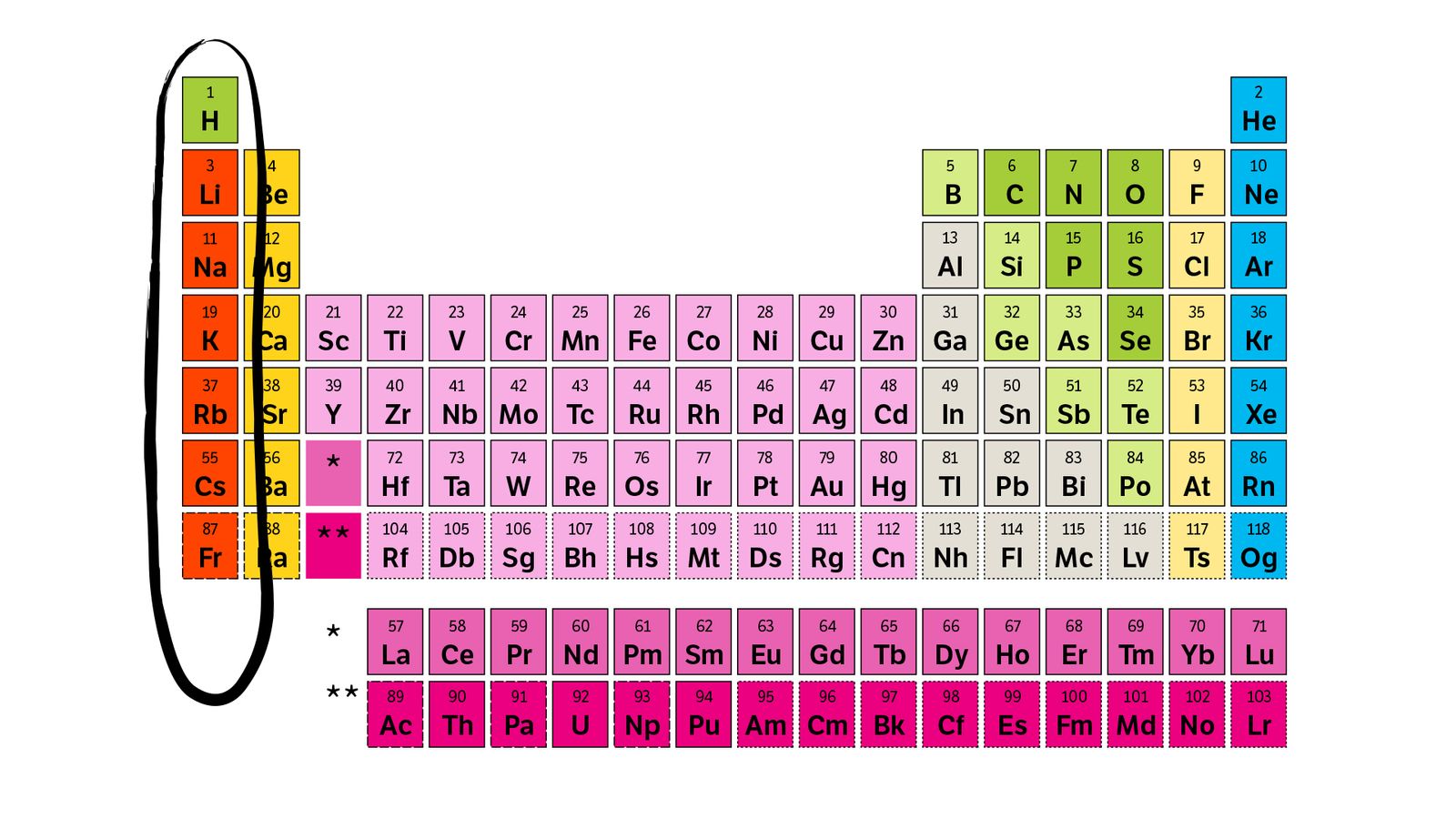
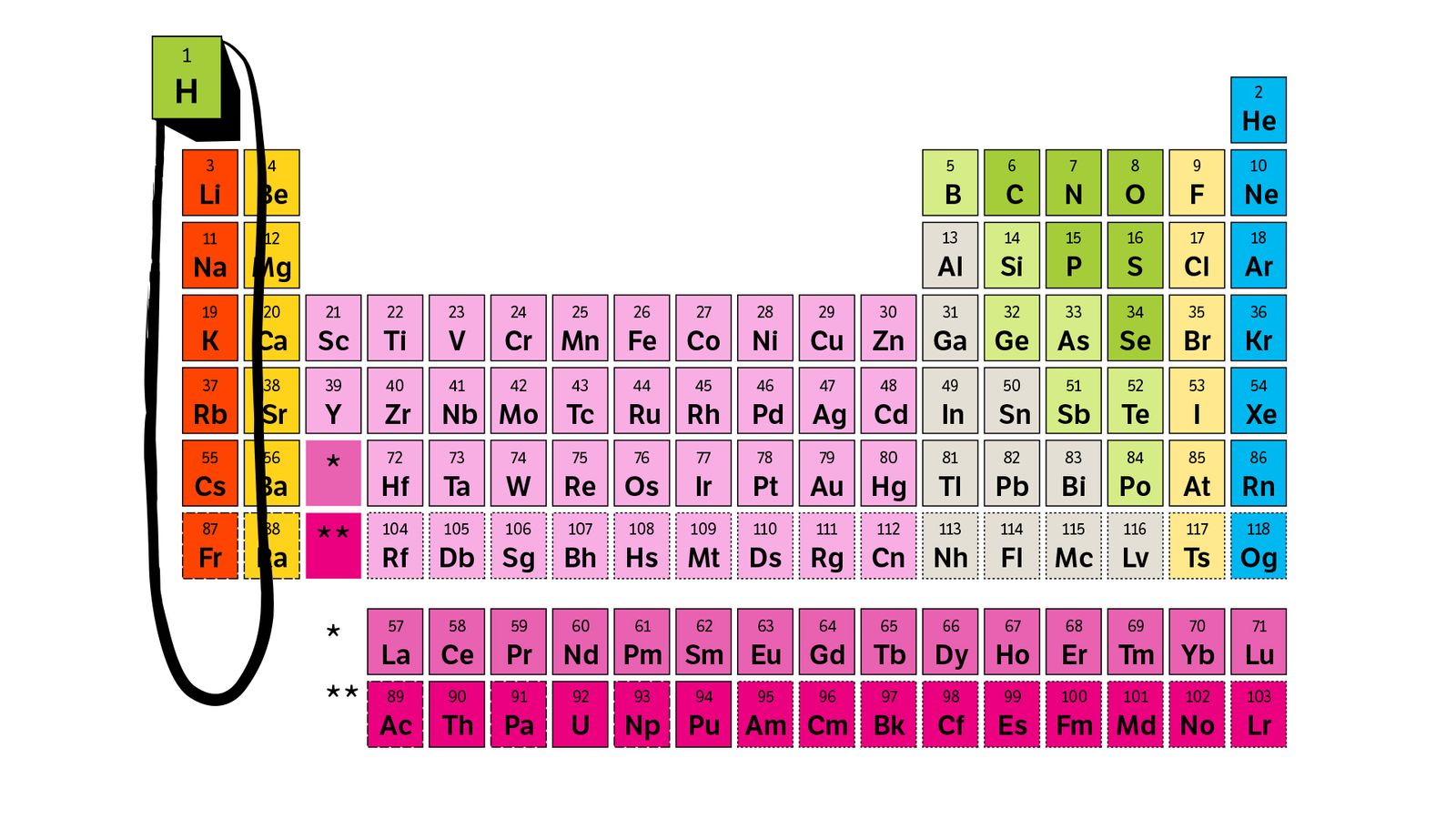
Eksempel: Hydrogen, som er plassert helt øverst til venstre har ett elektronskall med ett elektron.
Francium, det radioaktive grunnstoffet du ser nederst til venstre, har sju elektronskall med til sammen 87 elektroner, men bare ett i det ytterste skallet.
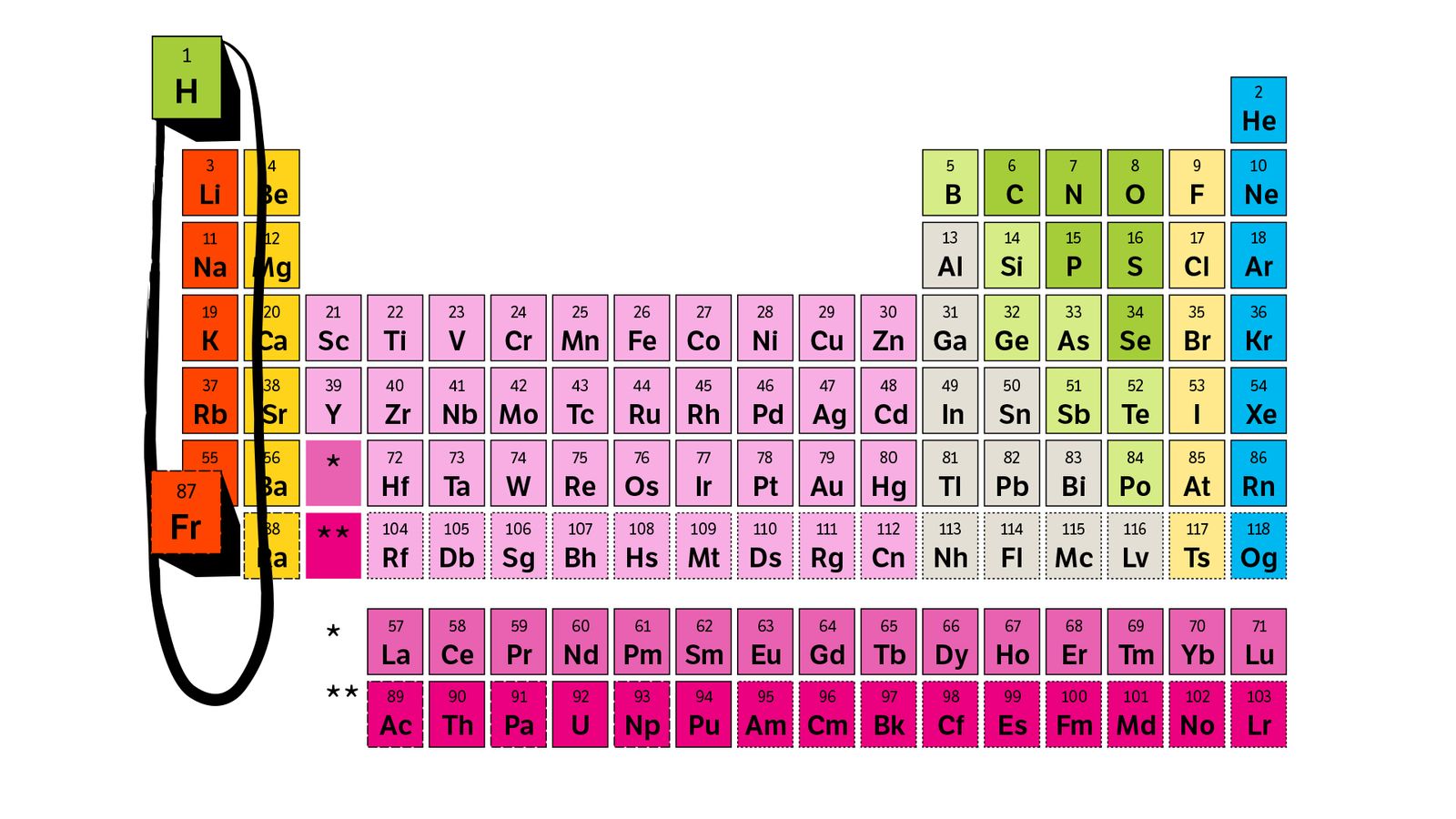
Grunnstoffenes oppførsel styres i stor grad av hvor mange elektroner de har i ytterskallet. For eksempel er stoffene i gruppe én, der vi blant annet finner nevnte hydrogen og francium, veldig reaktive. Det enslige elektronet i ytterste skall gjør at de gjerne vil binde seg med andre grunnstoff – atomer trives best med fulle elektronskall.
Gruppa helt til høyre i periodesystemet består av grunnstoff som har helt fullt elektronytterskall, for eksempel helium og radon. Disse kalles edelgasser, og er i motsetning til stoffene med bare ett elektron i ytterskallet særdeles lite interesserte i å inngå kjemiske forbindelser med andre grunnstoff.
De horisontale radene viser hvilke grunnstoff som befinner seg i samme periode. Vi har sju perioder, hver periode inneholder grunnstoff som har like mange elektronskall.
Hydrogen og helium har som nevnt helt ulike kjemiske egenskaper, men de har like mange elektronskall, bare ett, og er derfor i samme periode.

PERIODISERING: Det periodiske system har fått navnet sitt etter de horisontale periodene. Grunnstoffenes oppførsel gjentar seg med forutsigbare intervaller, og hvert intervall kalles en periode.
Foto: NRKSå langt er alt bare fryd og gammen. Naturen har tilsynelatende lagd et oversiktlig sett med ulike byggeklosser som formelig roper om å bli satt i et intuitivt og pedagogisk system.
Riktig så enkelt er det ikke.
Hydrogenproblemet
Problemene starter allerede ved det første grunnstoffet, hydrogen. Universets vanligste grunnstoff passer rett og slett ikke inn i periodesystemet.
Navnet på gruppe én avslører noe av trøbbelet – hydrogen og alkalimetaller. Litium, natrium og kalium er alkalimetaller, hydrogen er ikke et metall i det hele tatt, det er en gass.
Hydrogen, med sitt enslige elektron, har like mange elektroner i ytterskallet som sine metalliske gruppekamerater, altså ett. Men siden det første elektronskallet bare har plass til to elektroner, mangler det også bare ett på å ha fullt ytterskall, akkurat som grunnstoffene i gruppe 17. Denne ytterskallet halvfullt/halvtomt-situasjonen bidrar til at det er vanskelig å sette hydrogen i bås.
– Det er umulig å gjøre alle til lags når fysikken sier én ting og de kjemiske egenskapene sier noe annet.
Rolf Jonas Persson er fysiker ved NTNU, og en av initiativtakerne bak Periodesystemets år ved samme universitet. Han forklarer at hydrogen strengt tatt ikke ligner på noe annet grunnstoff, og at det egentlig ikke har noe naturlig plass i et periodesystem basert på fysiske egenskaper.
– En fysiker hadde nok satt opp periodesystemet på en litt annen måte. Mendelejev så først på kjemien, deretter på fysikken. Skal både kjemien og fysikken ivaretas er det nesten umulig å få til det i et todimensjonalt system.

Persson har bygd ulike legovarianter av periodesystemet. Denne versjonen, som viser stoffenes tetthet, står utstilt på NTNU sammen med flere andre modeller.
Foto: Erlend Lånke Solbu / Erlend Lånke SolbuRelativitetens rariteter
Persson er særlig opptatt av såkalte relativistiske effekter i periodesystemet, noe som bringer oss videre til to andre grunnstoffer som skiller seg litt ut – gull og kvikksølv
Først: Einsteins relativitetsteori lar seg ikke forklare på et par linjer, men helt ekstremt forenkla kan vi si at den forklarer hvordan naturen oppfører seg når ting går veldig fort, er veldig store, eller veldig tunge.
- Her kan du lese mer om relativitetsteorien:
- Her kan du lese mer om hvordan gullet i verden ble danna:
Elektroner beveger seg i utgangspunktet ekstremt kjapt. Høyere atomnummer betyr flere protoner i kjernen, flere protoner i kjernen betyr at elektronene må bevege seg enda kjappere for å kompensere for kreftene som trekker dem inn mot kjernen.
Når du kommer til gull og kvikksølv, grunnstoff nummer 79 og 80, går elektronene så kjapt at relativitetsteorien må blandes inn for å forklare hvorfor stoffene ser ut som de gjør. For kvikksølvets del har den relativistiske effekten gjort stoffet flytende i romtemperatur, veldig ulikt sine naboer i systemet. Gull har på sin side blitt gult, som eneste metall. Begge stoffene passer helt fint inn rent kjemisk, mens de fysisk skiller seg ut.
Trøbbel i gruppe tre
Den kanskje største konflikten knytta til periodesystemdesignet handler om den evig problematiske gruppe tre, og de to radene som er forvist til et liv litt på utsiden. For å forklare hvorfor de har havna der, må vi prate litt om elektronskallkonfigurasjon.
I de øverste radene går alt intuitivt og greit for seg. På rad og rekke fyller grunnstoffene opp elektronskallene, fra innerst til ytterst. Dette fungerer strålende, i hvert fall for en liten stund. Elektronskallene er nemlig delt opp i orbitaler. Vi kan tenke på orbitalene som områder som huser elektroner med forskjellig energinivå, noe som gjør det hele litt mer innvikla.
Når vi kommer til grunnstoff nummer 57, lantan, dukker det opp et nytt orbital, f-orbitalet. For å få alt til å gå opp, og for å unngå at periodesystemet blir uhensiktsmessig bredt, er det tatt drastiske grep. 15 grunnstoff i periode seks og 15 grunnstoff i periode sju er plassert under resten av periodesystemet, selv om de strengt tatt hører hjemme på innsida.

FORVIST: Lantanoidene og aktinoidene blir stort sett plassert under periodesystemet, men de hører fortsatt hjemme i periode seks og sju.
Foto: NRKDet visuelle utenforskapet er ikke hovedproblemet, selv om den nåværende løsninga ikke nødvendigvis er optimal. Det store spørsmålet er hvilke grunnstoff som skal stå først i den såkalte f-blokka. Ser vi på elektronskallkonfigurasjonen er det naturlig å beholde den som den er, anført av lantan og actinium. Ser man derimot på egenskaper som atomradius og smeltepunkt er det mer passende å la Lutetium og Lawrencium lede an.
Dette har vært en såpass het potet at International Union of Pure and Applied Chemistry (IUPAC) har nedsatt ei gruppe som skal ta stilling til akkurat problemet. Når IUPAC prater lyttes det, det er gjengen som blant annet utvikler standardene for navngiving av grunnstoffene.
Lars Öhrström, professor ved Chalmers Tekniska Högskola i Göteborg, er én av seks medlemmer i gruppa som har jobba med dette siden 2016. Han kan ikke si noe om hvor langt de er unna å komme med en anbefaling, men forteller at det beste argumentet for å forandre på periodesystemet er det faktum at f-blokka noen ganger består av 28 grunnstoff, andre ganger av 30. Enkelte periodesystem inkluderer lantan og actinium i gruppe tre, rett under scandium og yttrium. Andre lar de plassene stå åpne, og henviser grunnstoff nummer 57 og 89 til f-blokka.
– Fra et pedagogisk perspektiv er det lite tilfredsstillende, for ikke å si forvirrende.
Men Öhrström har også argumenter for å beholde systemet som det er.
– Det er vel som med mekanikk, et stivt og rigid system går lettere i stykker. Hvis man beholder en viss fleksibilitet og tvetydighet holder det kanskje lenger. Den nåværende varianten fungerer bra.
– Tullprat
Periodesystemet Mendelejev la grunnlaget for har blitt standardmåten å sortere grunnstoff på, men det er ikke fordi det ikke finnes alternativer. Periodesystemer finnes i alle former, farger, fasonger og nøyaktighetsgrader. Mange er bygd etter det samme prinsippet, bare med ulikt design. Flere er spiralforma, enkelte er tredimensjonale. Noen er veldig visuelle, andre er stort sett bare tekst og tall.
Theodore Benfeys snegleforma spiralvariant starter med hydrogen innerst, og jobber seg utover. Stoffene som i dag er i f-blokka har fått sin egen utstikker, det har også overgangsmetallene.
Tony Grainger har lagd denne todimensjonale fremstillinga av et tredimensjonalt periodesystem.
Ungdommen er også representert i Leach sin database - 12 år gamle Marco Piazzalunga har foreslått en helt rund variant.
Mark Leach, som er kjemiprofessor ved Manchester Metropolitan University, har tatt på seg oppgaven med å samle så mange varianter som mulig. I The Internet Database of Periodic Tables har han foreløpig godt over tusen, men det betyr ikke at han ivrer etter permanente endringer:
– Periodesystemet kommer ikke til å forandres. Den nåværende versjonen med perioder og grupper fungerer utmerket, og alt snakket om at det skal eksistere bedre måter å gjøre det på er tullprat.
Klar tale fra Leach.
Persson ved NTNU er ikke fullt så kategorisk, men heller ikke han tror på forandring.
– Periodesystemet er et kraftfullt pedagogisk instrument, og det vi bruker nå har blitt ikonisk. Jeg tror nok ikke det kommer til å endres i lærebøker de neste 100 åra.
Gammel vane kan være vond å vende, også i vitenskapens verden.
– Vi bruker det fordi vi har brukt det lenge. Det var der da vi starta
Fortsatt ikke fått nok av periodesystemet? Da anbefaler vi to nye populærvitenskapelige bøker i sin helhet via til emnet – «Menneskets grunnstoffer» av Anja Røyne, og «Genier, sjarlataner og 50 bøtter med urin» av Eivind Torgersen.
Takk til New Scientist for inspirasjon.
Sjekk også ut periodesystemet her.







