Krystallenes skjønnhet har gjort at de er flittig brukt som smykker og prydgjenstander. Enkelte krystaller brukes slik de forekommer i naturen (for eksempel beryll og bergkrystall), mens andre slipes og bearbeides (for eksempel diamanter).
Smykker med slike bearbeidede krystaller (edelstener) kan komme opp i svimlende summer, men visste du at krystaller har også mer ”lavmælte” bruksområder?
Mikroskop og solcellepanel

Tre prøver av kalsitt. Den fargeløse er fri for kjemiske urenheter. Den grønne prøven får trolig sin farge fra spormengder av magnesium (Fe). Den rosa prøven får sin farge fra manganforurensninger. (Foto: A. O. Harstad, NHM, UiO)
Særlig innenfor teknologi og teknologisk utvikling har krystaller spilt en sentral rolle. Den danske vitenskapsmannen Erasmus Bartholin oppdaget i 1669 lysets dobbeltbrytning gjennom glassklare kalsittkrystaller (såkalt ”Iceland spar”) og dette førte etter hvert til utviklingen av det første polarisasjonsmikroskopet.
Krystaller av kvarts ble brukt i radioen under krigen og har senere fått en sentral rolle innen frekvenskontroll av urverk (jfr. kvartsuret) og dataprosessorer. Krystaller blir også brukt som råmateriale til videreforedling av ulike kjemiske elementer.
Et eksempel på dette er bruken av superren kvarts som råmateriale for silisium (Si) til bruk i produksjon av solcellepanel.
Krystallenes svært plane overflater utnyttes også, for eksempel til fokusering og sentrering av laserlys (ofte brukes det her laboratoriefremstilte krystaller).
4000 ulike mineraler
Alle Jordens bergarter er satt sammen av ett eller flere ulike mineraler, f.eks. består bergarten granitt av de tre mineralene kvarts, feltspat og glimmer. Vi sier at noe er et mineral når et bestemt sett av kjemiske bestanddeler (f.eks. silisium og oksygen i kvarts, SiO2) har en regelmessig, romlig (3D) ordning.
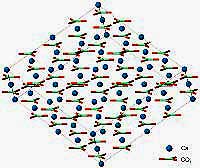
Krystallstrukturen til mineralet kalsitt består av en regelmessig oppbygning av kalsium (Ca) og sammenkoblede karbon- og oksygenenheter (CO3). Den regelmessige strukturen gjentar seg i tre dimensjoner.
En slik oppbygning av atomer i tre dimensjoner kalles en krystallstruktur og vi sier at slike materialer er krystallinske. Den nøyaktige utformingen av krystallstrukturen (også kalt krystallgitter) bestemmes av de ulike ionenes (atomenes) ladning, størrelse og kjemiske binding.
Krystallstrukturen er altså mineralets indre oppbygning og det er krystallstrukturen som bestemmer et minerals ulike fysiske egenskaper, slik som hardhet (styrken på bindingene mellom atomene), densitet (atomenes natur, samt hvor tett de sitter i gitteret) og optiske egenskaper (lysets brytning i krystallgitteret). Total kjenner vi i dag ca. 4000 ulike mineraler.

En relativt vanlig krystallform for kalsitt, satt sammen av et heksagonalt prisme (basisform) og det vanlige romboeder (toppen). (Foto: P. E. Aas, NHM, UiO)
Hva er et krystall?
Med begrepene mineral, krystallstruktur og krystallinsk friskt i minne, kan vi gå over til å definere hva en krystall er.
Vi sier at vi har en krystall når et mineral har en ytre begrensning bestående av et sett med plane flater som forholder seg strengt geometrisk til hverandre.
Hvilke krystallflater et gitt mineral vil utvikle, avhenger av mineralets krystallstruktur, samt de fysiske og kjemiske forholdene under krystallveksten (temperatur, trykk, samt sammensetningen til væsken, gassen eller smelten som krystallen vokste fra).
Trenger et hulrom
En annen forutsetning for at krystaller skal kunne dannes er tilstedeværelsen av et åpent (hul)rom som krystallene kan vokse inn i.
Når krystaller dekker tak og vegger i et slikt hulrom, kaller vi det for et druserom. Det har vist seg at alle mulige krystaller kan innordnes i seks eller syv forskjellige krystallsystemer, nemlig det kubiske (isometriske), tetragonale, heksagonale, (orto)rombiske, trikline og monokline. Det syvende er det trigonale, som av mange oppfattes som en undergruppe av det heksagonale system.
32 ulike klasser
Krystallsystemene er ytterligere fordelt på 32 forskjellige krystallklasser. Et mineral tilhørende et gitt krystallsystem (og krystallklasse) kan utvikle en rekke ulike krystallformer, eller sett av krystallformer, og det er dette som gir opphavet til det store mangfoldet i krystallutforminger vi ser hos de ulike mineralene.
Ordet krystall stammer fra det greske ordet ”krystallos” som betyr is, og har sitt opphav fra den tiden man trodde at bergkrystaller (kvarts, SiO2) var dannet ved kraftig nedkjøling av vann (muligens fra observasjoner av iskrystalldannelse?).
Vann viktig
Langt de fleste krystaller vi finner i naturen er dannet fra vandige væsker med ulike kjemiske sammensetninger. På sin ferd gjennom bergartene vil vann kunne løse opp ulike kjemiske stoffer. Hva som løses opp i en slik væske avhenger av bergartene vannet er i kontakt med, samt temperatur, trykk og væskens surhetsgrad (pH).
Generelt er det slik at varme væsker kan løse opp større mengder materiale enn kalde væsker. Dersom en varm væske med et høy innhold av oppløste stoffer (for eksempel silisium-oksygen komplekser, SiO44-) blir avkjølt, vil dens evne til å holde på det oppløste materialet svekkes og væsken vil begynne å ”felle ut” stoffer som er i overskudd.
De komplekserte ionene vil da kunne organisere seg i små strukturelle enheter (for eksempel Si2O76-). Når slike enheter fester seg sammen og vokser til en tredimensjonal struktur, får vi dannet små kim som etter hvert kan utvikle seg til større krystaller.
Lagvis påbygning
Krystallenes videre vekst skjer ved en lagvis påbygning av materiale i samsvar med det gjeldende krystallgitteret og det etablerte settet med krystallflater. Som geometrisk form representerer krystallen en tilstand der atomene og flatene er ordnet slik at krystallens samlede overflateenergi representerer et minimum.
En minimering av overflateenergi er vanlig i de fleste naturlige systemer, og således kan man si at krystaller representerer resultatet av ”perfekte” naturlige systemer.

En marmorbergart fra Cararra i Italia. Denne marmoren består nesten utelukkende (99 %) av mineralet kalsitt, som kan sees som små glinsende korn (Foto: A. O. Harstad, NHM, UiO)
Kalsittkrystaller
Mineralet kalsitt (kalkspat) har den kjemiske sammensetningen CaCO3 og en krystallstruktur bestående av vekslende lag med Ca-atomer og CO3-grupper.
I naturen finner vi hovedsakelig kalsitt som hovedbestanddel i kalkstein og marmor. I tillegg finner vi ofte krystaller av kalsitt i en rekke andre geologiske miljøer. Som mineral stikker kalsitt seg ut ved at dets krystaller kan ha et enormt antall ulike utseender, og mer enn 2500 ulike kalsittkrystaller er til nå beskrevet.
Kalsitt skiller seg ut
Kalsitt tilhører en krystallgruppe som begrenser antallet generelle krystallformer til seks stykker.
Det at vi likevel kjenner så mange ulike utseender for kalsittkrystaller, skyldes at man kan ha utviklet krystallflater fra flere ulike krystallformer i èn og samme krystall.
Også med hensyn til farge skiller kalsitt seg fra mange andre mineraler (og krystaller) ved at kalsittkrystaller kan opptre i alle mulige farger, fra fargeløse (klare, gjennomsiktige) til sorte. Som for alle andre krystaller skyldes variasjonen i farge uregelmessigheter i krystallgitteret.
Slike uregelmessigheter kan være ”fremmede” atomer (for eksempel små mengder jern, Fe) eller defekter/feil i gitterets struktur (feilplasserte elektroner).
Kalsitt som har en klar lysgul farge kalles ofte ”honningkalsitt” og skyldes at noen av Ca-atomene i krystallstrukturen er byttet ut med Fe-atomer. Den enorme variasjonen i form og farge som vi finner hos krystaller av kalsitt har gjort at kalsittkrystaller er et høyt skattet mineral for samlere.
Fakta og myter
I den senere tid har krystaller fått en sentral rolle innenfor alternativ medisin/behandling. Her brukes krystaller i ”krystall healing” hvor de blir tilegnet ulike helbredende egenskaper.
Ofte kan man lese at forskjellige krystaller kan helbrede alt fra stress, angst og søvnløshet til langt mer alvorlige lidelser. Dessverre er det slik at disse ”healerne” ofte bruker vitenskapelige (for eksempel mineralogiske) forklaringer på krystallenes påståtte helsebringende effekt. Dette er svært uheldig, da det per dags dato ikke finnes en eneste etterprøvbar vitenskapelig studie som kan dokumentere slike evner hos krystaller.
I en slik sammenheng er det viktig å skille mellom tro og vitenskap, slik at de to ikke blir forvekslet. Folk må gjerne tro at en krystall kan gjøre dem friske, men de skal være klar over at dette ikke på noen som helst måte skyldes dokumenterbare egenskaper hos krystallene. Dagens vitenskapelige nivå er så høyt at dersom krystaller hadde innehatt slike egenskaper, ville dette vært kjent vitenskapelig for lengst.






